Что такое карбиды, их роль в производстве и свойства
Карбиды — это соединения металлов и неметаллов с углеродом. Обычно в таких соединениях углерод имеет большую электроотрицательность, чем второй элемент, что позволяет исключить из группы оксиды, галогены и другие углеродные соединения.
Это твердые тугоплавкие вещества, нелетучие и нерастворимые. В основном они обладают разнообразными свойствами: некоторые, например, карбид золота, может взорваться при попытке пересыпать его, а некоторые из соединений, например, бора, циркония, титана, кремния и вольфрама, по твердости превосходят алмаз и не поддаются действию кислот и растворителей. Содержание
Историческая справкаПервое необычное углеродное соединение, похожее на карбид, было получено в начале XIX века англичанином Дэви. Это был карбид калия. Далее в 1863 году был найден неустойчивый карбид меди, через 15 лет — карбид железа. Официально соединения «появились» только в конце XIX века — к ним приложил руку француз Анри Муассон. Он получал соединения при помощи вольтовой дуги в электрической печи, которую он сам и придумал. Для этого использовались нагретый до раскаленного состояния древесный уголь, чистые металлы и их оксиды. Однако за несколько лет до Муассона в метеоритах был обнаружен минерал когенит — смесь карбидов кобальта, железа и никеля. В некотором смысле эта находка помогла ответить на вопрос «Что такое карбиды?». Свойства соединенийКак и другие элементы, карбиды обладают определенным набором свойств, которые делают их популярным материалом на рынке строительства и машиностроения.  Высокая твердость — в отличие от чистого металла соединения являются наиболее твердыми, что позволяет использовать их в самых разных областях; В зависимости от металла и неметалла элементы обладают разнообразными свойствами, которые меняются в зависимости от начальных данных. Виды карбидовВсе вещества можно разделить на три группы: 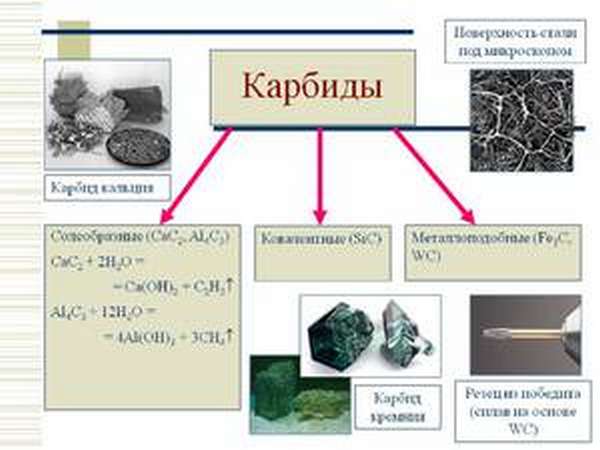 Солеобразные или ионные — это соединения, образованные металлами I и II групп, а также алюминием, РЗЭ и актиноидами. Их получают непосредственно из элементов или путем восстановления оксидов углерода Обычно они разлагаются водой и кислотами, при этом происходит выделение углеводорода и остается гидроксид металла. Обладают высокой температурой плавления. В свою очередь ионные соединения делятся на: ПрименениеЭлементы используют, чтобы придать чугуну и разного вида сталям твердость, повысить их износоустойчивость. Карбиды вольфрама и титана, как наиболее твердые и тугоплавкие варианты, применяют для изготовление режущих инструментов, а также для получения сверхтвердых материалов. Благодаря хорошим химическим и физическим свойствам, вещества используют в качестве компонента огнеупорных материалов, стержней сопротивления электронагревательных приборов и в качестве абразивного материала.  Карбид кальция также называют карбидом для сварки. Это идеальное вещество для сварочных работ: при контакте с водой оно выделяет ацетилен — летучий газ, являющийся основой кислородной сварки, металлизации, резки и напайки. Иначе говоря, при обработке металла соединение вступает в реакцию и начинает выделять огромное количество тепла и ацетилена, который поддерживает горение. Температура при этом может достигать 3150 градусов Цельсия. При работе с веществом необходимо строго придерживаться правил безопасности: правильно хранить смесь, помнить о том, что он легко загорается, стараться не контактировать с ядовитой полью.
ВыводВ зависимости от металла соединения обладают внушительным рядом свойств, которые используют в разных видах производства, в основном, в машиностроении, металлообработке и тому подобных отраслях.
|
Загрузка. Пожалуйста, подождите...